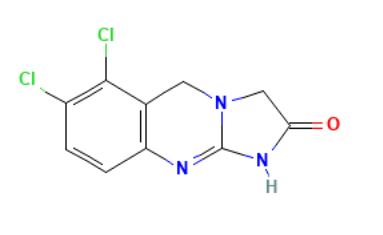
ANAGRELIDE – XAGRID
Denominazione del farmaco:
Xagrid 0,5 mg capsule rigide.
SCHEDA TECNICA XAGRID (RCP) (fonte: EMA – 27/02/2022)
INDICAZIONI
Xagrid è indicato per la riduzione della conta piastrinica elevata nei pazienti con trombocitemia essenziale (TE) a rischio, i quali mostrano intolleranza nei riguardi della loro attuale terapia, oppure la cui conta piastrinica elevata non possa essere ridotta a un livello accettabile con l’attuale terapia.
Paziente a rischio
Per paziente con trombocitemia essenziale a rischio si intende un paziente che presenti una o più delle caratteristiche riportate di seguito:
- Età > 60 anni, oppure
- Conta piastrinica > 1.000 x 109/L, oppure
- Storia di eventi tromboemorragici.
CONTROINDICAZIONI
- Ipersensibilità ad anagrelide o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1 dell’RCP.
- Pazienti con insufficienza epatica moderata o severa.
- Pazienti con compromissione renale moderata o severa (clearance della creatinina < 50 ml/min).
Meccanismo d’azione
Non è noto il meccanismo preciso con cui anagrelide porta alla riduzione della conta piastrinica. Negli studi condotti in colture cellulari, anagrelide ha soppresso l’espressione dei fattori di trascrizione quali GATA-1 e FOG-1, necessari per la megacariocitopoiesi, provocando in definitiva una riduzione della produzione piastrinica.
Gli studi in vitro sulla megacariocitopoiesi umana hanno stabilito che le azioni inibitorie di anagrelide sulla piastrinogenesi nell’uomo sono mediate tramite il ritardo della maturazione dei megacariociti, e inoltre tramite la loro riduzione in termini di dimensioni e ploidia. Sono emerse prove di azioni simili in vivo, da campioni di biopsie midollari dei pazienti trattati.
Anagrelide è un inibitore della fosfodieresterasi III c-AMP dipendente.
Anagrelide su PubMed ==> da QUI
Anagrelide sul sito della FDA ==> da QUI
Anagrelide sul sito della Cochrane ==> da QUI
Anagrelide sul motore di ricerca del “Nationali Institutes of Health” degli USA ==> da QUI
NOTA INFORMATIVA IMPORTANTE SU XAGRID (ANAGRELIDE CLORIDRATO DEL 22/02/2022 (fonte; AIFA)
Vi è un aumentato rischio di complicanze trombotiche, compreso l’infarto cerebrale, in caso di interruzione improvvisa di anagrelide.
L’interruzione improvvisa del trattamento deve essere evitata a causa del rischio di un improvviso aumento della conta piastrinica e di complicanze trombotiche potenzialmente fatali, come l’infarto cerebrale.
In caso di interruzione del dosaggio o sospensione del trattamento, monitorare frequentemente la conta piastrinica (fare riferimento al paragrafo 4.4 dell’RCP).
Istruire i pazienti su come riconoscere i primi segni e sintomi indicativi di complicanze trombotiche, come un infarto cerebrale, e a rivolgersi al medico nel caso in cui si verificassero tali sintomi.
Nota Informativa importante AIFA su Xagrid (Anagrelide cloridrato) del 22/02/2022 in PDF
Con determina n. 163/2014 l’Anagrelide è stato inserito “nell’elenco dei medicinali erogabili a totale carico del Servizio sanitario nazionale, ai sensi della legge 23 dicembre 1996, n. 648, per la terapia di prima linea della trombocitemia essenziale in pazienti di età inferiore ai 40 anni” nel rispetto delle condizioni per esso indicate nell’allegato 1 (che riporto qui sotto) che fa parte integrante della determinazione:
Denominazione: Anagrelide
Indicazione terapeutica: Terapia di prima linea della trombocitemia essenziale in pazienti di età inferiore ai 40 anni.
Criteri di inclusione: pazienti con trombocitemia essenziale di età < 40 anni, con conta piastrinica > 1.000×109/l, e/o con storia di eventi trombo emorragici.
Criteri di esclusione: ipersensibilità ad anagrelide o ad uno dei suoi eccipienti; insufficienza epatica moderata o grave (transaminasi > 5 volte il limite superiore dei valori normali); insufficienza renale moderata o grave (clearance della creatinina < 50 ml/min); gravidanza, allattamento.
Periodo di prescrizione a totale carico del Servizio sanitario nazionale: fino a nuova determinazione dell’Agenzia Italiana del Farmaco.
Piano terapeutico: Il trattamento con Xagrid deve essere istituito da un medico esperto nel controllo della trombocitemia essenziale. La dose iniziale di anagrelide consigliata è di 1 mg/die, da somministrare per via orale in due dosi separate (0,5 mg/dose). Mantenere costante la dose iniziale per almeno una settimana. Dopo una settimana è possibile titolare la dose, caso per caso, per pervenire alla dose minima efficace per ridurre e/o mantenere la conta piastrinica al di sotto di 600 x 109/l, e se possibile a un livello fra 150 x 109/l e 400 x 109/l.
Non aumentare la dose di oltre 0,5 mg/die nell’arco della stessa settimana; la dose singola massima consigliata non deve superare 2,5 mg. Durante lo sviluppo clinico sono state utilizzate dosi pari a 10 mg/die. Controllare regolarmente gli effetti del trattamento con anagrelide. Se la dose iniziale è > 1 mg/die, procedere a conteggi delle piastrine ogni due giorni nella prima settimana di trattamento, e almeno una volta alla settimana in seguito, fino a giungere a una dose stabile di mantenimento. Tipicamente si osserverà un calo della conta piastrinica entro 14 – 21 giorni dall’avvio del trattamento. Nella maggior parte dei pazienti sarà possibile osservare una risposta terapeutica adeguata e stabile con l’assunzione di 1-3 mg/die.
Altre condizioni da osservare: le modalità previste dagli articoli 4, 5, 6 del provvedimento datato 20 luglio 2000 citato in premessa, in relazione a:
- art. 4: istituzione del registro, rilevamento e trasmissione dei dati di monitoraggio clinico ed informazioni riguardo a sospensioni del trattamento (mediante apposita scheda come da Provvedimento 31 gennaio 2001, pubblicato sulla Gazzetta Ufficiale n. 70 del 24 marzo 2001);
- art. 5: acquisizione del consenso informato, modalità di prescrizione e di dispensazione del medicinale;
- art. 6: rilevamento e trasmissione dei dati di spesa.
DATI DA INSERIRE NEL REGISTRO
| prima di iniziare il trattamento | durante il trattamento | alla fine del trattamento | |
| Emocromo | x | x | |
| Conta Leucocitaria | x | x | |
| Conta piastrinica | x | x | |
| Esame cardiovascolare (visita) | x | x | |
| Elettrocardiogramma Basale: QTc | x | x | |
| Ecocardiogramma | x | x | |
| Elettroliti : Na, K, Cl | x | x | |
| Funzionalità Epatica: AST, ALT | x | x | |
| Funzionalità Renale (cretinina, Azotemia) | x | x | |
| Esame clinico accurato | x | x |
COSTO E REGIME DI DISPENSAZIONE
- Xagrid cps 0,5 mg – 100 capsule
- prezzo ex factory: € 416,66 (IVA esclusa)
- Classe: “H”