DIMETILFUMARATO – TECFIDERA
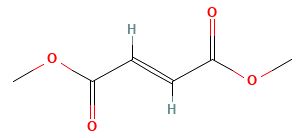
formula di struttura del dimetilfumarato (tecfidera) fonte: pubchem
formula chimica: C6H8O4
nome IUPAC: dimethyl (E)-but-2-enedioate
Nome del farmaco e formulazioni:
- Tecfidera 120 mg capsule rigide gastroresistenti
- Tecfidera 240 mg capsule rigide gastroresistenti
SCHEDA TECNICA TECFIDERA (RCP) – Fonte: EMA 04/02/2023
riassunto della relazione pubblica europea di valutazione (EPAR) per Tecfidera ad uso del pubblico
INDICAZIONI
Tecfidera è indicato per il trattamento di pazienti adulti e pediatrici di età pari o superiore a 13 anni con sclerosi multipla recidivante-remittente (SM-RR)
(vedere paragrafo 5.1 dell’RCP per importanti informazioni sulle popolazioni per le quali l’efficacia è stata dimostrata).
CONTROINDICAZIONI
Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1 dell’RCP.
Leucoencefalopatia multifocale progressiva (Progressive multifocal leukoencephalopathy, PML) sospetta o confermata.
Meccanismo d’azione
Il meccanismo con cui il dimetilfumarato esercita gli effetti terapeutici nella sclerosi multipla non è pienamente compreso. Gli studi preclinici indicano che le risposte farmacodinamiche del dimetilfumarato risultano principalmente mediate attraverso l’attivazione della via di trascrizione del fattore nucleare 2 eritroide 2-correlato (Nrf2). È stato dimostrato che nei pazienti il dimetilfumarato provoca la sovraregolazione (up-regulation) dei geni antiossidanti dipendenti da Nrf2-dipendenti (ad es. NAD(P)H deidrogenasi, chinone 1; [NQO1]).
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA’ REGOLATORIE EUROPEE E L’AGENZIA ITALIANA DEL FARMACO (AIFA) (NOVEMBRE 2015)
TECFIDERA® (DIMETILFUMARATO): NUOVE MISURE PER MINIMIZZARE IL RISCHIO DI PML –POTENZIAMENTO DELLE NORME PER IL MONITORAGGIO E L’INTERRUZIONE
” …
Riassunto
Si raccomanda di intraprendere le seguenti azioni al fine di ridurre il rischio di PML:
- Prima di iniziare il trattamento con Tecfidera:
- assicurarsi che venga eseguito un emocromo completo (linfociti compresi)
- deve essere disponibile un esame di risonanza magnetica (MRI) basale (di norma entro 3 mesi dall’inizio del trattamento) da usare come riferimento
- consigliare i pazienti riguardo al rischio di PML, ai possibili sintomi clinici da riconoscere e alle azioni da intraprendere qualora insorga uno qualsiasi di questi sintomi.
- Dopo l’inizio del trattamento con Tecfidera:
- monitorare ogni 3 mesi l’emocromo completo, linfociti compresi
- a causa di un possibile aumento del rischio di PML, considerare l’interruzione di Tecfidera in pazienti con conte linfocitarie al di sotto di 0,5×109/L che persistano per più di 6 mesi (ovvero linfopenia severa e prolungata)
- qualora il trattamento venga interrotto a causa di una linfopenia, proseguire il monitoraggio dei pazienti fino a che i valori linfocitari rientrano nella normalità.
- Altre considerazioni:
Si tenga presente che la PML può verificarsi soltanto in presenza di un’infezione da virus di John-Cunningham (JCV). Qualora vengano effettuati test sul JCV, si deve tenere in considerazione che l’influenza della linfopenia sull’accuratezza del test per gli anticorpi anti-JCV non è stata studiata nei pazienti trattati con Tecfidera. È inoltre necessario tenere presente che un test negativo per la presenza di anticorpi anti-JCV (in presenza di conte linfocitarie normali) non preclude la possibilità di infezione da JCVin futuro. - Qualora il trattamento venga proseguito in pazienti con linfopenia severa e prolungata, si raccomanda un potenziamento del livello di vigilanza per l’eventuale insorgenza di PML:
- consigliare nuovamente i pazienti e coloro che si occupano dei pazienti riguardo al rischio di PML in presenza di fattori di rischio e ricordare loro i primi sintomi clinici da riconoscere
- sottoporre i pazienti a monitoraggio per verificare la presenza di segni e sintomi o l’insorgenza di nuove disfunzioni neurologiche (ad es. disfunzione motoria, sintomi cognitivi o psichiatrici). Bisogna tener presente che la PML si può manifestare con caratteristiche simili a quelle della sclerosi multipla, poiché si tratta in entrambi i casi di patologie demielinizzanti
- valutare la necessità di ulteriori esami di risonanza magnetica (MRI) nell’ambito di un aumento del livello di vigilanza relativa alla PML, in accordo con le raccomandazioni nazionali e locali.
- In qualsiasi paziente, qualora si sospetti l’insorgenza di PML interrompere immediatamente il trattamento con Tecfidera ed eseguire gli esami del caso.
…”
La “Nota Informativa Importante su Tecfidera (dimetilfumarato) (19/11/2015)” in formato PDF
Comunicazione EMA su Tecfidera (26/10/2015)
Tecfidera: raccomandazioni aggiornate per minimizzare il rischio di rara infezione cerebrale PML
Analoghe raccomandazioni si applicano anche agli altri medicinali a base di fumarato.
“ … L’Agenzia europea per i medicinali (EMA) ha emanato una nuova raccomandazione per medici e pazienti al fine di minimizzare i rischi di leucoencefalopatia multifocale progressiva (PML) nei pazienti con sclerosi multipla trattati con Tecfidera (dimetilfumarato). … Ad oggi si sono verificati 3 casi di PML in pazienti trattati con Tecfidera che in precedenza non avevano assunto altri farmaci noti per essere associati al rischio di PML …
L’EMA raccomanda attualmente che venga eseguito un esame emocromocitometrico completo prima di iniziare il trattamento con Tecfidera, e ogni 3 mesi durante il trattamento. Inoltre, deve essere eseguita una RMN basale come riferimento (di norma entro 3 mesi). Se durante il trattamento i linfociti scendono a livelli molto bassi per più di 6 mesi, il medico dovrebbe considerare l’interruzione del trattamento con Tecfidera. Se il trattamento viene continuato, i pazienti devono essere attentamente monitorati
… Alcuni pazienti che sono in trattamento con Fumaderm, medicinale indicato per la psoriasi, i cui principi attivi comprendono dimetil-fumarato, lo stesso principio attivo di Tecfidera, possono anche presentare prolungati bassi livelli di linfociti, e di conseguenza questi pazienti sono soggetti a più alto rischio di PML se hanno contratto il virus di JC. Pertanto sulla base dei dati disponibili provenienti dalle segnalazioni di PML ricevute per Fumaderm, le raccomandazioni relative al monitoraggio dei livelli di globuli bianchi sono applicabili anche per questi medicinali. Fumaderm è commercializzato solo in Germania. …”
Per il documento completo in formato PDF da QUI
Nota Informativa Importante su Tecfidera (dimetilfumarato)
Nota Informativa Importante redatta su richiesta del Comitato di valutazione dei rischi per la farmacovigilanza (PRAC) del giorno 4 novembre 2014 (03/12/2014)
Tecfidera (dimetilfumarato): insorgenza di leucoencefalopatia multifocale progressiva (PML) in un paziente con linfocitopenia severa e prolungata.
Gentile Dottoressa/Egregio Dottore,
In accordo con l’Agenzia europea per i medicinali (EMA), Biogen Idec desidera comunicarle importanti informazioni di sicurezza riguardanti un caso di leucoencefalopatia multifocale progressiva (PML) correlato all’uso di Tecfidera nel trattamento della sclerosi multipla:
Riassunto
- Nell’ottobre 2014 un caso fatale di leucoencefalopatia multifocale progressiva (PML) in corso di linfocitopenia severa e prolungata è stato segnalato in un paziente che aveva ricevuto Tecfidera per 4,5 anni. Questo è il primo caso di PML associato a Tecfidera. È necessario informare i pazienti del rischio di questa grave patologia.
- La linfocitopenia è una reazione avversa nota di Tecfidera e i pazienti in trattamento devono essere monitorati regolarmente. Una valutazione della conta ematica completa (emocromo con formula), compresa la conta linfocitaria deve essere effettuata regolarmente e a intervalli ravvicinati, se clinicamente indicato.
- I pazienti che ricevono Tecfidera e sviluppano linfocitopenia devono essere sottoposti a stretto e frequente monitoraggio per rilevare i segni e i sintomi della disfunzione neurologica.
- Quando si sospetta la PML, il trattamento con Tecfidera deve essere interrotto immediatamente.
Ulteriori informazioni
Tecfidera è autorizzato per il trattamento della sclerosi multipla recidivante-remittente nei pazienti adulti. Tecfidera può causare linfocitopenia con una riduzione osservata delle conte linfocitarie durante gli studi clinici del 30% circa.
I pazienti in trattamento con Tecfidera devono essere sottoposti a stretto monitoraggio e le valutazioni della conta ematica completa (emocromo con formula), compresa la conta linfocitaria devono essere effettuate regolarmente e a intervalli ravvicinati, se clinicamente indicato.
Un caso di leucoencefalopatia multifocale progressiva (PML) è stato segnalato nell’ottobre 2014. Il paziente partecipava allo studio clinico in aperto ENDORSE e ha ricevuto la terapia con Tecfidera per 4,5 anni. Durante il trattamento con Tecfidera, il paziente ha sviluppato una linfocitopenia severa e prolungata (oltre 3,5 anni di durata). La linfocitopenia prolungata può essere associata a un maggiore rischio di PML. Le conte linfocitarie oscillavano tra 200 e 580 cellule/μL [principalmente Common Toxicity Criteria (CTC) Grado 3 (tra 200 e 500 cellule/μL) a partire da gennaio 2011]. Il paziente è deceduto a causa di complicanze associate al deterioramento delle condizioni neurologiche e a polmonite da aspirazione.
La leucoencefalopatia multifocale progressiva (PML) è una rara e grave infezione cerebrale causata dal virus JC. Questo virus è comunemente presente nella popolazione generale ma causa la PML solo se il sistema immunitario è stato indebolito. La PML si manifesta come malattia demielinizzante con sintomi simili alla sclerosi multipla. Se i sintomi sono suggestivi di PML o se esistono dubbi al riguardo, il trattamento con Tecfidera deve essere interrotto e devono essere effettuati ulteriori accertamenti.
I medici devono informare in modo appropriato i propri pazienti sul rischio di PML.
Questo è il primo caso di PML associato a Tecfidera. In passato, altri casi di PML sono stati segnalati con l’uso di esteri dell’acido fumarico nel trattamento di pazienti linfopenici con psoriasi, benché nella maggior parte di questi casi non è stata chiarita la relazione causale (ad es. se altri rischi per la PML erano presenti).
Biogen Idec sta attualmente valutando le evidenze disponibili e lavorerà con l’EMA per valutare le appropriate modifiche alle informazioni per la prescrizione, comprendenti ulteriori indicazioni sulla gestione della linfocitopenia severa e prolungata e del rischio di PML. Qualsiasi nuova raccomandazione rivolta agli operatori sanitari ed ai pazienti sarà comunicata tempestivamente.
Richiesta di segnalazione
Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta associata all’uso di Tecfidera in conformità con i requisiti nazionali tramite il sistema nazionale di segnalazione all’indirizzo www.agenziafarmaco.gov.it/it/responsabili.
Punto di contatto aziendale
I contatti per ulteriori informazioni sono forniti nelle informazioni sul prodotto del medicinale (RCP e Foglio illustrativo) nel sito: http://www.EMA.europa.eu/EMA/.
Per il documento in formato PDF da QUI
Dimetilfumarato sul PubMed ==> da QUI
Dimetilfumarato sul sito della FDA ==> da QUI
Dimetilfumarato e sclerosi multipla su Google Scholar (ricerca globale) ==> da QUI
Dimetilfumarato e sclerosi multipla su Google Scholar (ricerca in lingua italiana) ==> da QUI
Regime di dispensazione
Medicinale soggetto a prescrizione medica limitativa, vendibile al pubblico su prescrizione di specialisti operanti nei Centri designati dalle Regioni per prescrizione dei farmaci di Nota 65 (RRL).